Книга: Самая главная молекула. От структуры ДНК к биомедицине XXI века
Силы, стабилизирующие двойную спираль
| <<< Назад Правы ли Уотсон и Крик? |
Вперед >>> Z-форма |
Силы, стабилизирующие двойную спираль
Ответ на вопрос, поставленный в конце предыдущего раздела, может показаться тривиальным. В самом деле, очевидно, что те силы, которые обеспечивают образование комплементарных пар, А•Т и Г•Ц (рис. 38), и удерживают две цепочки друг около друга. Речь идет о так называемых водородных связях (Н-связях). Эти связи по своей силе занимают промежуточное положение между ковалентными связями, соединяющими атомы в молекулы, и чисто межмолекулярными взаимодействиями. Н-связи играют огромную роль и в ДНК, и в РНК, и в белках, и просто в чистой воде, особенно во льду. Именно способность молекул Н2О образовывать друг с другом Н-связи обусловливает многие аномальные свойства воды, делающие ее столь необычной субстанцией.
Итак, кажется очевидным, что именно Н-связи между комплементарными основаниями удерживают две цепочки ДНК вместе. Так долгое время и считалось. В главе 3 было рассказано о плавлении ДНК, т. е. о расхождении комплементарных цепей при нагревании раствора ДНК. В полном соответствии с представлением о том, что водородные связи удерживают комплементарные цепи друг с другом, ДНК с большим содержанием Г•Ц-пар плавится при более высокой температуре. В самом деле, именно это и следовало ожидать, ведь в Г•Ц-паре имеется три Н-связи, а в А•Т-паре – только две (рис. 38). Причем температура плавления ДНК растет строго линейно с увеличением доли Г•Ц-пар в молекуле. Эта строго линейная зависимость ясно свидетельствовала о том, что стабильность участка двойной спирали зависит только от количества Н-связей в участке и не зависит от того, как Г•Ц – и А•Т-пары распределены вдоль цепи.
С другой стороны, те же данные по плавлению ДНК свидетельствовали о существенном взаимодействии между соседствующими вдоль цепи парами оснований, которое получило название стэкинг-взаимодействия (от английского слова stack, что значит «штабель, стопка»). Получалось, что по каким-то непонятным причинам все 10 стэкинг-взаимодействий между соседними парами оснований практически одинаковы, иначе бы нарушалась линейная зависимость температуры плавления от Г•Ц-содержания. Заметим, что всего контактов между соседними парами 16, но из-за правила комплементарности разных контактов 10: идентичны контакты АГ / ЦТ, ГА / ТЦ, АЦ / ГТ, ЦА / ТГ, АА / ТТ и ГГ / ЦЦ. Из данных по плавлению удалось извлечь различия в стэкинг-взаимодействиях между разными контактами, но эти различия рассматривались как малая поправка к основному эффекту: была полная уверенность, что двойная спираль стабилизируется главным образом Н-связями между коплементарными парами и различие в температуре плавления разных участков ДНК практически целиком определяется различием в содержании Г•Ц-пар между этими участками. На самом деле, как стало постепенно ясно, из данных по плавлению нельзя извлечь отдельно вклад в стабильность от спаривания оснований и вклад от стэкинг-взаимодействий. Так что уверенность в определяющей роли спаривания оснований основывалась не на твердом знании, а на знаменитом принципе, известном как «бритва Оккамы» (мы уже упоминали этот принцип в главе 4), т. е. казавшееся простейшим объяснение данных по плавлению ДНК принималось за истину.
Разделить вклады в стабильность двойной спирали от спаривания оснований и от стэкинг-взаимодействий удалось в моей группе в Бостонском университете в 2004–2006 годах. Эта работа была выполнена моим тогдашним постдоком, выпускницей МФТИ, защитившей диссертацию в Университете Торонто, Катей Протозановой и моим аспирантом Петей Яковчуком.
Идея работы возникла совершенно случайно, в ходе изучения коротких синтетических молекул ДНК, содержащих однонитевой разрыв («ник»). Мы обратили внимание на то, что такие молекулы движутся в геле при электрофорезе слегка медленнее, чем молекулы без разрыва. Оказалось, что причина в том, что молекулы с ником часть времени проводят в состоянии стэкинга, т. е. движутся так же, как и молекулы без разрыва, а часть времени проводят в состоянии разрушенного стэкинг-взаимодействия, как проиллюстрировано на рис. 40, и движутся в геле медленнее. Соотношение этих двух состояний должно экспоненциально зависеть от энергии стэкинга, согласно известному распределению Больцмана (точнее, речь идет не об энергии как таковой, а о свободной энергии). Таким образом, приготовив 16 синтетических молекул, отличающихся только двумя парами оснований слева и справа от места ника, мы определили энергию стэкинг-взаимодействий для всех 16 контактов. Важным инструментом, который мы при этом использовали, были специальные ферменты – никазы, способные совершенно точно наносить ник в определенном месте двухнитевой ДНК. Собственно, в ходе изучения работы никаз мы и наткнулись на эффект замедленного движения молекул с ником в геле.
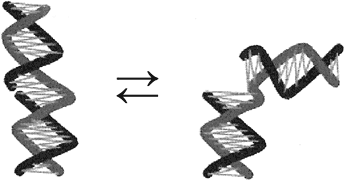
Рис. 40. ДНК, содержащая однонитевой разрыв («ник»), может находиться в двух состояниях, в одном из которых сохраняется стэкинг-взаимодействие между парами оснований, расположенными по обе стороны от ника, а в другом это взаимодействие разрушено
Что же в итоге оказалось? Мы определили энергии всех контактов, и они менялись от контакта к контакту так же, как те значения энергии, которые были найдены ранее из данных по плавлению ДНК. Но когда мы вычли из общей энергии стабилизации двойной спирали энергию стэкинг-взаимодействий и тем самым определили вклад Н-связей внутри комплементарных пар в энергию стабилизации, нас ждал большой сюрприз. Оказалось, что этот вклад практически равен нулю! Точнее, А•Т-пары слегка дестабилизируют двойную спираль, а Г•Ц-пары слегка стабилизируют, но вклад тех и других гораздо меньше, чем стабилизирующий эффект стэкинг-взаимодействий. Иными словами, открывшаяся картина меняла устоявшееся представление об относительной роли Н-связей и стэкинг-взаимодействий в стабилизации двойной спирали на 180 градусов.
Но как такое могло быть? Как это так: Н-связи, считавшиеся такими важными и в ДНК, и в РНК, и в белках, вдруг оказались не важными для стабильности двойной спирали? И разве из железно установленного факта линейной зависимости температуры плавления ДНК от Г•Ц-содержания не следовало однозначно, что вклад стэкинг-взаимодействий мал по сравнению с вкладом Н-связей? Давайте разберемся по порядку.
Говоря о стабильности, мы всегда имеем в виду не саму энергию двойной спирали (точнее, не свободную энергию), а разницу между энергией двойной спирали и двух разделенных цепей ДНК. Так что мы должны сравнивать ситуацию с Н-связями в этих двух состояниях. Но когда основания перестают образовывать комплементарные пары, их группы, способные к образованию Н-связей, немедленно образуют Н-связи с молекулами воды. Наши данные лишь означали, что этот баланс оказывается близким к нулю, но это не так уж удивительно. Это никак не умаляет роль Н-связей в уотсон-криковских парах оснований: ведь если бы Н-связи не образовывались внутри двойной спирали, но продолжали образовываться с молекулами воды в раскрытых парах, то это приводило бы к такой страшной невыгодности спирального состояния, что никакие стэкинг-взаимодействия не могли бы ничем помочь. Точно так же стэкинг-взаимодействия не выручают, если по каким-то причинам в ДНК образуется некомплементарная пара, скажем, А против А: тогда возникает дефект, который устраняется репарирующей системой клетки.
Хорошо, с Н-связями разобрались, ну а как же быть с линейной зависимостью температуры плавления от Г•Ц-содержания? Ведь если стабильность определяется стэкинг-взаимодействиями, которые разные для разных контактов, то наряду с линейным членом должен быть квадратичный член, а его нет, согласно эксперименту. Кажется, Эйнштейн как-то сказал, что Природа не злонамеренна, но коварна. Это тот самый случай, когда проявилось коварство Природы: она как будто нарочно ввела нас в заблуждение о том, какие силы стабилизируют «самую главную молекулу». Если предположить, что различные нуклеотиды распределены вдоль ДНК случайным образом, вычислить в этом предположении коэффициент при квадратичном члене и подставить значения стэкинг-взаимодействий, полученные нами в опытах с короткими ДНК, содержащими ник, то этот коэффициент получится практически равным нулю. Иными словами, стэкинг-взаимодействия для разных контактов таковы, что температура плавления ДНК со случайной последовательностью должна строго линейно зависеть от Г•Ц-содержания, т. е. имитировать ситуацию, будто водородные связи, а не стэкинг-взаимодействия определяют стабильность двойной спирали. А поскольку данные о температурах плавления были получены для бактериальных геномов, в которых нет мусорной ДНК, в отличие от эукариот (о мусорной ДНК речь пойдет в главе 12), то предположение о случайном распределении нуклеотидов вполне реалистично, как реалистично предположение о случайности распределения букв в осмысленном лингвистическом тексте.
Ну и последнее. Если дело не в том, что у Г•Ц-пары три Н-связи, а у А•Т-пары две, то как объяснить рост температуры плавления с Г•Ц-содержанием ДНК? Очень просто. Согласно нашим данным, стэкинг-взаимодействия для контактов, содержащих Г•Ц-пары, сильнее, чем для контактов, состоящих только из А•Т-пар. Этим и объясняется рост температуры плавления с увеличением Г•Ц-содержания ДНК, а вовсе не тем, что у Г•Ц-пары больше Н-связей, чем у А•Т-пары.
Такой поворот на 180 градусов в фундаментальных научных представлениях принято называть сменой парадигмы. Обычно научная общественность реагирует весьма болезненно на подобные резкие повороты. Но странным образом с нашей работой такого не произошло: нам без проблем удалось опубликовать наши результаты в ведущих профессиональных журналах, и эти статьи очень интенсивно цитируются в научной литературе. По-видимому, приведенные выше аргументы оказались для научной общественности вполне убедительными.
| <<< Назад Правы ли Уотсон и Крик? |
Вперед >>> Z-форма |
- Красота, симметрия и сверхстимулы
- Тайна белой каемки
- 10. Эукариотическая клетка. Цитоплазма. Органоиды
- Полосатая кошка, пятнистая кошка
- 5. Заключительные замечания
- Принципы систематики и классификации микроорганизмов
- Побить русичей камнями или повесить на крюках, на скотобойне?
- Достижения эволюционной психологии
- Легендарные растения
- 6. ПРОИСХОЖДЕНИЕ ЦВЕТКА
- Северная Америка
- Как живут папуасы
