Книга: Популярная библиотека химических элементов. Книга вторая. Серебро — нильсборий
Лантан и его команда
| <<< Назад Коротко о применении лантана и его соединений |
Вперед >>> О минералах редких земель |
Разделы на этой странице:
Лантан и его команда
Сравнение лантана и лантаноидов со спортивной командой, возможно, кому-то покажется надуманным. Однако это сравнение ничуть не крамольнее таких известных определений, как «семейство лантаноидов» или «химические близнецы». Судите сами: у лантана и его команды единая форма (серебристо-белого цвета) и, как у хоккеистов, у всех есть защитная амуниция (из окисных пленок). Всем им природой отпущено примерно поровну (сходство предельно велико), но, как и в спорте, в силу разных причин «способности» реализуются в не одинаковой мере: одни «играют» лучше, другие хуже… И конечно, у каждого члена этой команды свои излюбленные «финты» и «приемы» — ферромагнитность гадолиния, например.
И по химическим свойствам лантаноиды все-таки не близнецы — иначе не удалось бы их разделить. Как в хорошей спортивной команде, они едины в главном и индивидуальны в частностях. Что же касается числа участников, то в разных играх разное число игроков, 14 — в пределах нормы…
Правда, было время, когда в эту «команду» рекомендовали почти полсотни кандидатов. Число открываемых лантаноподобных элементов росло с катастрофической быстротой. В составленном профессором Н.А. Фигуровским списке ложно открытых элементов больше всего лжелантаноидов. Ошибок не избежали даже крупные ученые — Мозандер, Лекок де Буабодран, Ауэр фон Вельсбах, Крукс, Урбен.
Непериодичность свойств лантана и его команды, выпадающей из строгой последовательности периодической системы, доставляла неприятности Менделееву. Но со временем все разрешилось. Вынести лантаноиды за пределы основной части таблицы первым предложил профессор Пражского университета Богуслав Францевич Браунер.
Д.И. Менделеев и Б.Ф. Браунер — чешский химик, первым предложивший выделить лантаноподобные элементы в «междупериодическую группу или узел в таблице»
«Надо быть таким знатоком «редких земель», каков Б.Ф. Браунер, чтобы разобраться в этом сложном, трудном и еще едва ли сколько-либо законченном предмете, в котором проверка затруднена не только своеобразностью и сходственностью многих начальных отношений, но и трудностями в получении самого природного материала», — писал Менделеев в 1902 г.
«Что касается систематики элементов редких земель и их места в периодической системе, то в настоящее время можно с уверенностью считать, что скандий, иттрий и лантан стоят в четных рядах III группы, как это следует из их атомных весов и объема их окисей… Прочие элементы редких земель образуют, вероятно, междупериодическую группу или узел в системе, где они следуют друг за другом по величине атомных весов». Это слова Браунера из статьи «Элементы редких земель», написанной для предпоследнего (1903 г.) прижизненного издания менделеевских «Основ химии».
Распутать «узел в системе» окончательно удалось только после того, как в основу менделеевском таблицы был положен новый, физически более точный критерий — заряд атомного ядра. Тогда стало ясно, что между лантаном и танталом могут поместиться всего 15 элементов, причем последний должен быть аналогом циркония. Этот элемент — гафний — был открыт Костером и Хевеши в 1923 г. Последний (по атомным номерам) лантаноид, лютеций, был обнаружен раньше — в 1907 г.
Причины общности свойств лантана и лантаноидов естественно искать в строении электронных оболочек их атомов.
По законам квантовой механики электроны могут вращаться вокруг ядер не по любым орбитам. Они как бы распределяются по слоям — оболочкам. Емкость этих оболочек, максимальное число электронов в них, определяется формулой ne=2N2, где не — число электронов, а N — номер оболочки, считая от ядра. Отсюда следует, что на первой оболочке может быть всего два электрона, па второй — восемь, на третьей — восемнадцать, на четвертой — тридцать два и т. д.
Уже в четвертом периоде таблицы Менделеева, начиная со скандия, «очередные» электроны попадают не в наружный четвертый слой, а в предыдущий. Именно поэтому у элементов с атомными номерами от 21 до 30 разница в свойствах не такая резкая, как у более легких элементов. Подобная же картина наблюдается в пятом периоде. И здесь, начиная с иттрия, новые электроны заполняют не пятую, а предпоследнюю, четвертую оболочку — при этом образуется еще один ряд так называемых переходных металлов. Перенеся эту аналогию на шестой период, было бы логично предположить, что, начиная с лантана (он аналог скандия и иттрия), и здесь будет происходить то же самое. Электроны, однако, не считаясь с нашей логикой, заполняют здесь не предпоследнюю, а третью снаружи оболочку, благо на ней есть вакансии. Согласно формуле ne=2N2, на этой оболочке — четвертой от ядра — может быть 32 электрона. Сюда, за редким исключением, и попадают «новые» электроны очередных лантаноидов. А поскольку химические свойства элемента определяются прежде всего строением наружных электронных оболочек, свойства лантаноидов оказываются еще более близкими, чем свойства переходных металлов.
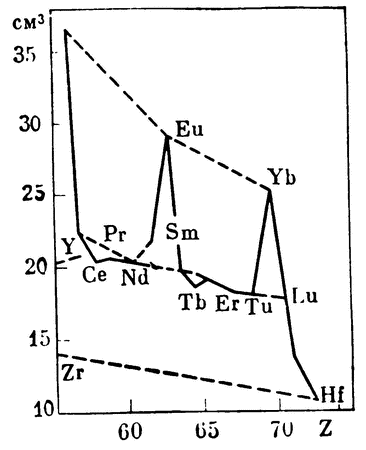
Кривая атомных объемов редкоземельных элементов. На ней два максимума, образуемых элементами, проявляющими валентность 2+ (европием и иттербием). Напротив, церий, неодим, тербий и другие элементы, которые могут быть четырехвалентными, имеют минимальные атомные объемы
Как и положено элементам III группы, лантаноиды обычно трехвалентны. Но некоторые из них могут проявлять и другую валентность: церий, празеодим и тербий — 4+; самарий, европий и иттербий — 2+.
Аномальные валентности лантаноидов исследовал и объяснил немецкий химик Вильгельм Клемм. По рентгеновским спектрам он определил основные параметры их кристаллов и атомные объемы. На кривой атомных объемов явно выражены максимумы (европий, иттербий) и менее резко — минимумы (церий, тербий). Празеодим и самарий тоже выпадают, хотя и не так сильно, из ряда, определяемого плавно ниспадающей кривой. Поэтому первый «тяготеет» к малообъемным церию и тербию, а второй — к крупным европию и иттербию. Элементы с большими атомными объемами крепче удерживают электроны, и потому бывают лишь трех- или даже двухвалентными. В «малообъемных» атомах, напротив, один из «внутренних» электронов заключен в оболочке недостаточно прочно — потому атомы церия, празеодима и тербия могут быть четырехвалентными.
В работах Клемма дано и физическое обоснование давно сложившегося разделения редкоземельных элементов на две подгруппы — цериевую и иттриевую. В первую входят лантан и лантаноиды от церия до гадолиния, во вторую — иттрий и лантаноиды от тербия до лютеция. Отличие между элементами двух этих групп — направление спинов у электронов, заполняющих главную для лантаноидов четвертую оболочку.
Спины — собственные моменты количества движения электронов — у первых имеют один и тот же знак; у вторых же половина электронов имеет спины одного знака, а половина — другого.
Но хватит об аномалиях, объяснимых только с помощью квантовой механики, — вернемся к закономерностям.
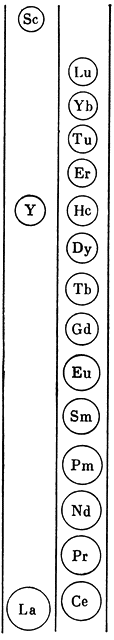
Лантаноидное сжатие: относительные размеры трехвалентных ионов редкоземельных элементов
Когда речь идет о лантаноидах, закономерности тоже порой кажутся алогичными. Пример тому — лантаноидное сжатие.
Лантаноидным сжатием называют открытое норвежским геохимиком Гольдшмидтом закономерное уменьшение размеров трехвалентного иона редкоземельных элементов — от лантана к лютецию. Казалось бы, все должно быть наоборот: в ядре атома церия на один протон больше, чем в ядре атома лантана; ядро празеодима больше, тем ядро церия, и так далее. Соответственно растет и число электронов, вращающихся вокруг ядра. И если представить атом таким, как его обычно рисуют па схемах, — в виде маленького диска, окруженного вытянутыми орбитами невидимых электронов, орбитами разных размеров, то, очевидно, прибыль электронов должна была бы увеличить размеры атома в целом. Или, если отбросить наружные электроны, число которых может быть неодинаковым, такая же закономерность должна наблюдаться в размерах трехвалентных ионов лантана и его команды.
Истинное положение вещей иллюстрирует диаграмма лантаноидного сжатия. Радиус трехвалентного иона лантана равен 1,22 А?, а такого же иона лютеция — всего 0,99 А?. Все не по логике, а как раз наоборот. Однако до физического смысла явления лантаноидного сжатия докопаться нетрудно и без квантовой механики, достаточно лишь вспомнить основные законы электромагнетизма.
Заряд ядра и число электронов вокруг пего растут параллельно. Сила притяжения между разноименными зарядами тоже растет: более тяжелое ядро сильное притягивает электроны, укорачивает их орбиты. A поскольку в атомах лантаноидов наиболее насыщены электронами глубинные орбиты, электрическое притяжение оказывает еще более сильное действие.
Близость ионных радиусов и общность химических свойств — вот главные причины совместного присутствия лантаноидов в минералах.
| <<< Назад Коротко о применении лантана и его соединений |
Вперед >>> О минералах редких земель |
